Una soluzione fisiologica (o soluzione salina) è una soluzione contenente cloruro di sodio (NaCl) disciolto in acqua purificata. Si tratta di un liquido utilizzato comunemente per infusioni endovenose, ma il suo utilizzo è ampio in ambito medico sanitario, basti pensare che la si trova per sciacquare le lenti a contatto, per alcune pratiche di igiene di irrigazione nasale e per riempire le protesi al seno.
Cos’è la soluzione fisiologica
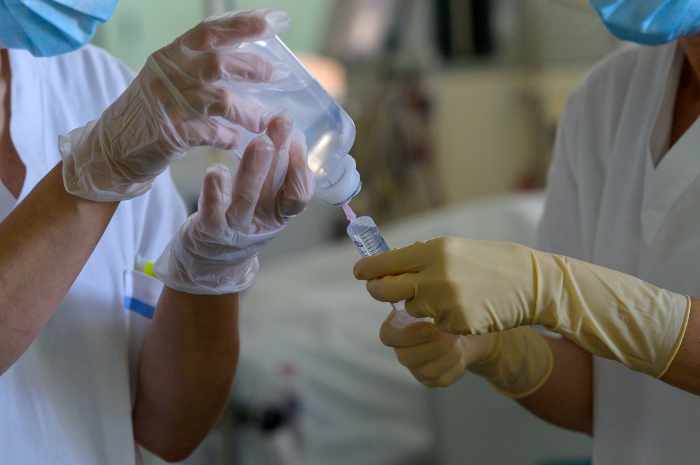
La soluzione fisiologica contiene lo 0,9% di NaCl
Nella sua concentrazione normale, la soluzione fisiologica è una soluzione contenente il 0,9% di NaCl, ovvero circa 9 g/L. Nonostante venga comunemente chiamata anche soluzione isotonica, il suo livello di osmolarità è leggermente più elevato rispetto al sangue (275 – 295 mOsm/L) in quanto pari a circa 300 mOsm/L. Tecnicamente, dunque, è inesatto affermare che questa soluzione sia isotonica rispetto al sangue.
A questa concentrazione è usata frequentemente per terapie endovenose su pazienti che non possono assumere fluidi oralmente e sono affetti da una disidratazione acuta.
La concentrazione normale di soluzione salina è solitamente il primo fluido utilizzato quando la disidratazione è abbastanza grave da minacciare la corretta circolazione del sangue; la ragione è che è il liquido più sicuro da assumere in grandi quantità.
Questo in quanto, alla concentrazione del 0,9%, la soluzione fisiologica si trova in equilibrio con il flusso sanguigno e non incide sul movimento dei liquidi verso e dalle cellule endoteliali delle vene. Per questo motivo, inoltre, si tratta della soluzione più utilizzata per la diluizione di farmaci.
In commercio esistono anche altre concentrazioni di soluzione che vengono utilizzate per altri scopi, ad esempio per fornire liquidi ad un paziente disidratato o per rispondere ai bisogni quotidiani di acqua e sali di un paziente che non può assumerli per via orale. Un esempio sono le soluzioni ipotoniche, nelle quali la concentrazione di tutti i soluti fluido extracellulare è inferiore a quella del fluido intracellulare.
Queste soluzioni possiedono un’osmolarità inferiore a 250-260 mOsm/l. Poiché le infusioni di una soluzione con bassa osmolarità possono creare problematiche quali citolisi, le soluzioni endovenose con concentrazioni minori sono solitamente accompagnate da glucosio, il quale mantiene un livello adeguato di osmolarità e allo stesso tempo apporta meno cloruro di sodio.
Siccome il peso molecolare del glucosio è maggiore, questo ha la stessa osmolarità della soluzione in concentrazione normale, ma immette meno sodio nella circolazione corporea. Viceversa, al fine di risolvere alcune disionie in commercio esistono anche soluzioni aventi un’osmolarità più elevata rispetto a quella sanguigna.
Queste soluzioni, dette ipertoniche, possiedono un’osmolarità superiore a 300-310 mOsm/l, con valori che raggiungono anche 500-1.000 mOsm/l. In questa classe di soluzioni l’osmolarità del soluto nel liquido extracellulare è maggiore rispetto a quello intracellulare. La pressione osmotica così generata fa sì che l’acqua presente all’interno della cellula passi alla parte extracellulare. In questo caso, l’organismo sarà obbligato a rilasciare acqua dalle cellule verso la circolazione sistemica, con conseguente diluizione degli ioni in eccesso.

















Commento (0)
Devi fare il login per lasciare un commento. Non sei iscritto ?